Minden évben április 17-én van a Rákellenes Világnap.
01 A rák előfordulásának áttekintése világszerte
Az utóbbi években, az emberek életkörülményeinek és mentális nyomásának folyamatos növekedésével, a daganatos megbetegedések előfordulása is évről évre növekszik.
A rosszindulatú daganatok (rákos megbetegedések) az egyik legjelentősebb közegészségügyi problémává váltak, amelyek komolyan veszélyeztetik a kínai lakosság egészségét. A legfrissebb statisztikai adatok szerint a rosszindulatú daganatok okozta halálesetek a lakosok összes halálokának 23,91%-át teszik ki, és a rosszindulatú daganatok előfordulása és halálozása az elmúlt tíz évben folyamatosan emelkedett. De a rák nem jelent „halálos ítéletet”. Az Egészségügyi Világszervezet egyértelműen rámutatott, hogy amennyiben korán felfedezik, a rákos megbetegedések 60–90%-a gyógyítható! A rákos megbetegedések egyharmada megelőzhető, egyharmada gyógyítható, és a rákos megbetegedések egyharmada kezelhető az élet meghosszabbítása érdekében.
02 Mi a daganat?
A tumor egy új organizmus, amely a helyi szövetsejtek proliferációjából jön létre különféle tumorogén faktorok hatására. Tanulmányok kimutatták, hogy a tumorsejtek metabolikus változásokon mennek keresztül, amelyek eltérnek a normál sejtekétől. Ugyanakkor a tumorsejtek képesek alkalmazkodni az anyagcsere-környezet változásaihoz a glikolízis és az oxidatív foszforiláció közötti váltás révén.
03 Egyénre szabott rákterápia
Az egyénre szabott rákkezelés a betegség célgénjeinek diagnózisára vonatkozó információkon és a bizonyítékokon alapuló orvosi kutatások eredményein alapul. Ez adja meg az alapot a betegek számára a helyes kezelési terv megszerzéséhez, ami a modern orvostudomány fejlődésének trendjévé vált. Klinikai vizsgálatok megerősítették, hogy a biomarkerek génmutációinak, a gén SNP-típusának, a gén- és fehérjeexpressziós állapotának kimutatásával a daganatos betegek biológiai mintáiban a gyógyszer hatékonyságának előrejelzése és a prognózis értékelése, valamint a klinikai egyénre szabott kezelés irányítása révén javítható a hatékonyság és csökkenthetők a mellékhatások, elősegítve az orvosi erőforrások racionális felhasználását.
A rák molekuláris vizsgálata három fő típusra osztható: diagnosztikai, örökletes és terápiás. A terápiás vizsgálat az úgynevezett „terápiás patológia” vagy személyre szabott orvoslás középpontjában áll, és egyre több antitest és kis molekulájú inhibitor alkalmazható a daganatok kezelésében, amelyek képesek a daganatspecifikus kulcsgéneket és jelátviteli útvonalakat megcélozni.
A tumorok molekuláris célzott terápiája a tumorsejtek markermolekuláit veszi célba, és beavatkozik a rákos sejtek folyamatába. Hatása főként a tumorsejtekre hat, a normál sejtekre csekély hatással van. A tumor növekedési faktor receptorok, a jelátviteli molekulák, a sejtciklus-fehérjék, az apoptózis-szabályozók, a proteolitikus enzimek, a vaszkuláris endoteliális növekedési faktor stb. mind felhasználhatók molekuláris célpontként a tumorterápiában. 2020. december 28-án a Nemzeti Egészségügyi és Orvosi Bizottság által kiadott "Adminisztratív intézkedések a daganatellenes gyógyszerek klinikai alkalmazására (kísérlet)" egyértelműen rámutatott, hogy: Az egyértelmű géncélpontokkal rendelkező gyógyszerek esetében a célgén-tesztelés után az alkalmazásuk elvét kell követni.
04 Tumor-célzott genetikai tesztelés
A daganatokban számos genetikai mutáció létezik, és a különböző típusú genetikai mutációk különböző célzott gyógyszereket igényelnek. A betegek csak a génmutáció típusának tisztázásával és a célzott gyógyszeres terápia helyes kiválasztásával profitálhatnak a kezelésből. Molekuláris detektálási módszereket alkalmaztak a daganatokban gyakran célzott gyógyszerekkel kapcsolatos gének variációinak kimutatására. A genetikai variánsok gyógyszerhatékonyságra gyakorolt hatásának elemzésével segíthetünk az orvosoknak a legmegfelelőbb személyre szabott kezelési terv kidolgozásában.
05 Megoldás
A Macro & Micro-Test kifejlesztett egy sor detektáló készletet a tumorgén kimutatására, amelyek átfogó megoldást kínálnak a tumorcélzott terápiára.
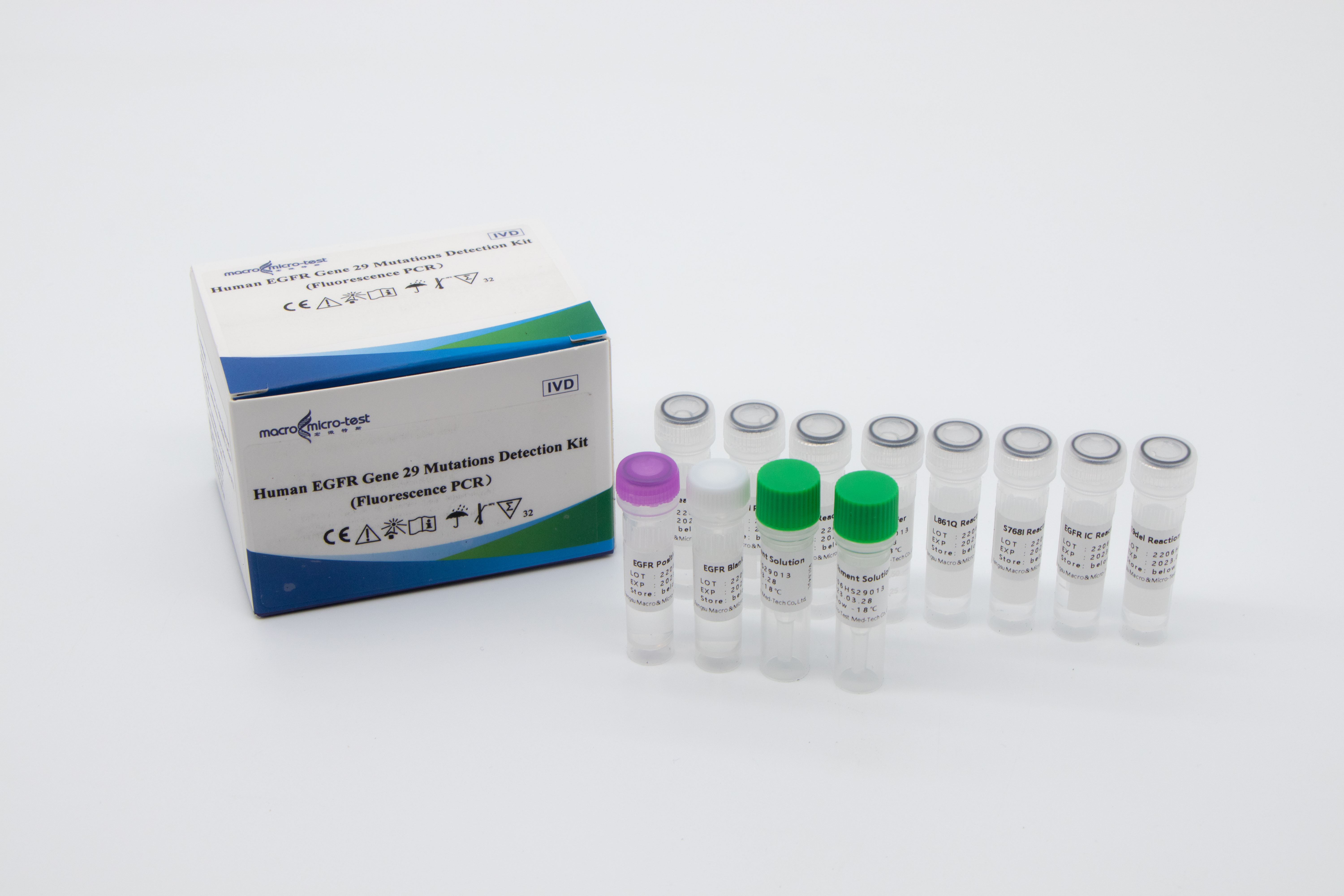
Humán EGFR gén 29 mutációk detektáló készlet (Fluoreszcencia PCR)
Ez a készlet az EGFR gén 18-21-es exonjaiban található gyakori mutációk in vitro kvalitatív kimutatására szolgál humán, nem kissejtes tüdőrákos betegektől származó mintákban.
1. A rendszer belső referencia minőségellenőrzést vezet be, amely átfogóan figyelemmel kíséri a kísérleti folyamatot és biztosítja a kísérlet minőségét.
2. Nagy érzékenység: A nukleinsav-reakcióoldat kimutatása stabilan képes kimutatni az 1%-os mutációs arányt 3 ng/μL vad típusú háttér mellett.
3. Nagy specificitás: Nincs keresztreakció vad típusú humán genomiális DNS-sel és más mutáns típusokkal.
 |  |
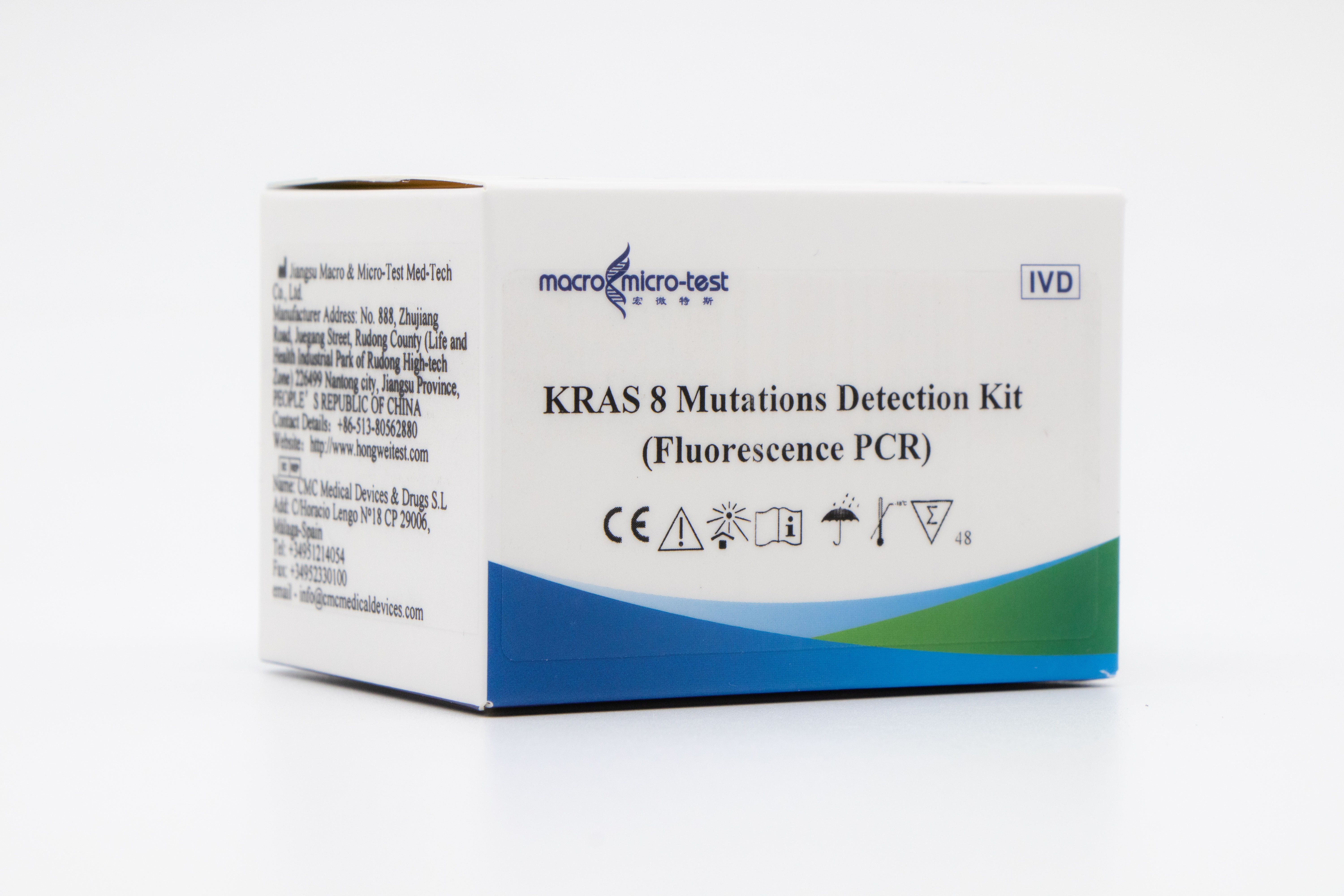
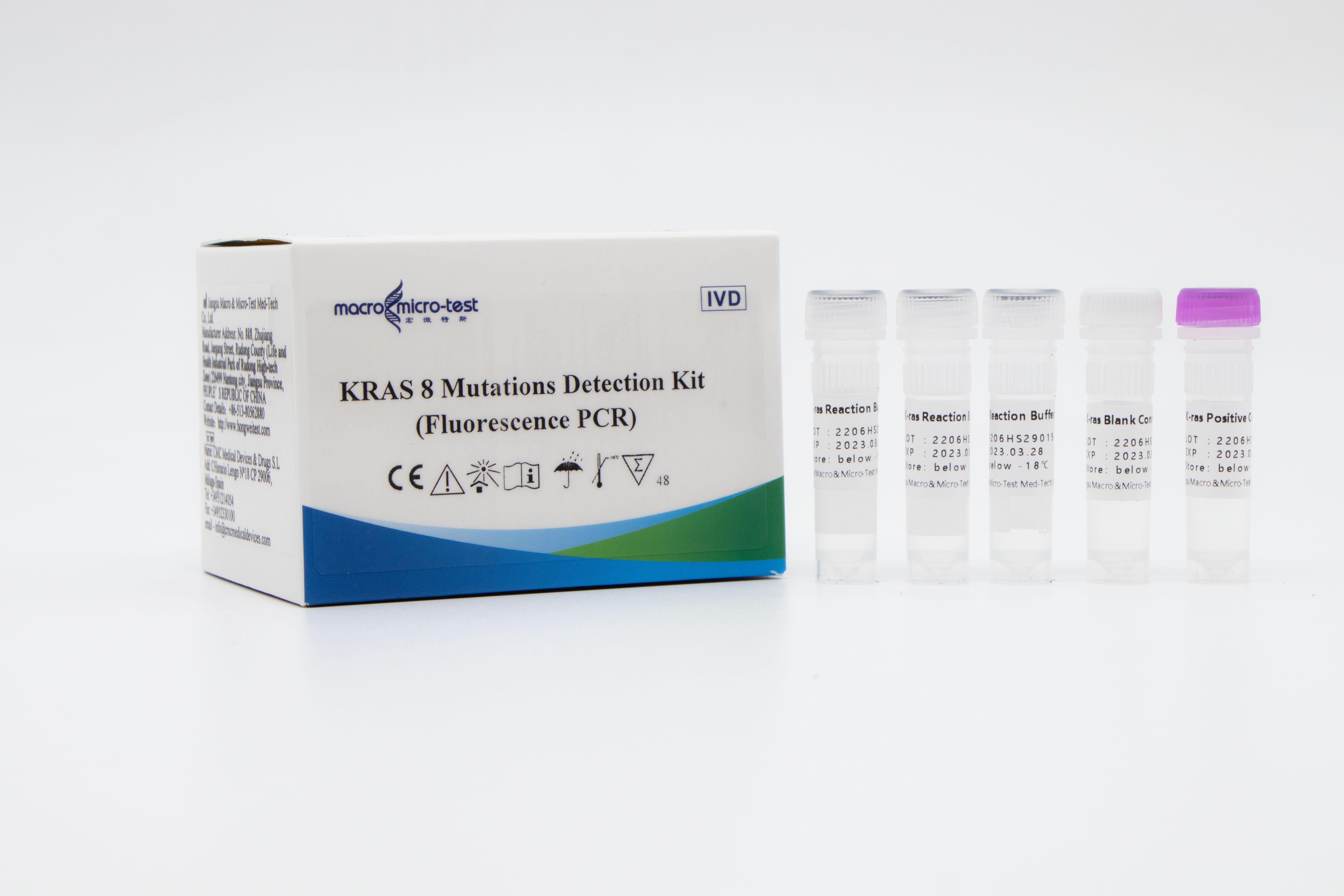
KRAS 8 mutáció detektáló készlet (fluoreszcencia PCR)
Ez a készlet a K-ras gén 12-es és 13-as kodonjaiban található 8 mutáció in vitro kvalitatív kimutatására szolgál humán paraffinba ágyazott patológiai metszetekből kivont DNS-ben.
1. A rendszer belső referencia minőségellenőrzést vezet be, amely átfogóan figyelemmel kíséri a kísérleti folyamatot és biztosítja a kísérlet minőségét.
2. Nagy érzékenység: A nukleinsav-reakcióoldat kimutatása stabilan képes kimutatni az 1%-os mutációs arányt 3 ng/μL vad típusú háttér mellett.
3. Nagy specificitás: Nincs keresztreakció vad típusú humán genomiális DNS-sel és más mutáns típusokkal.
 |  |
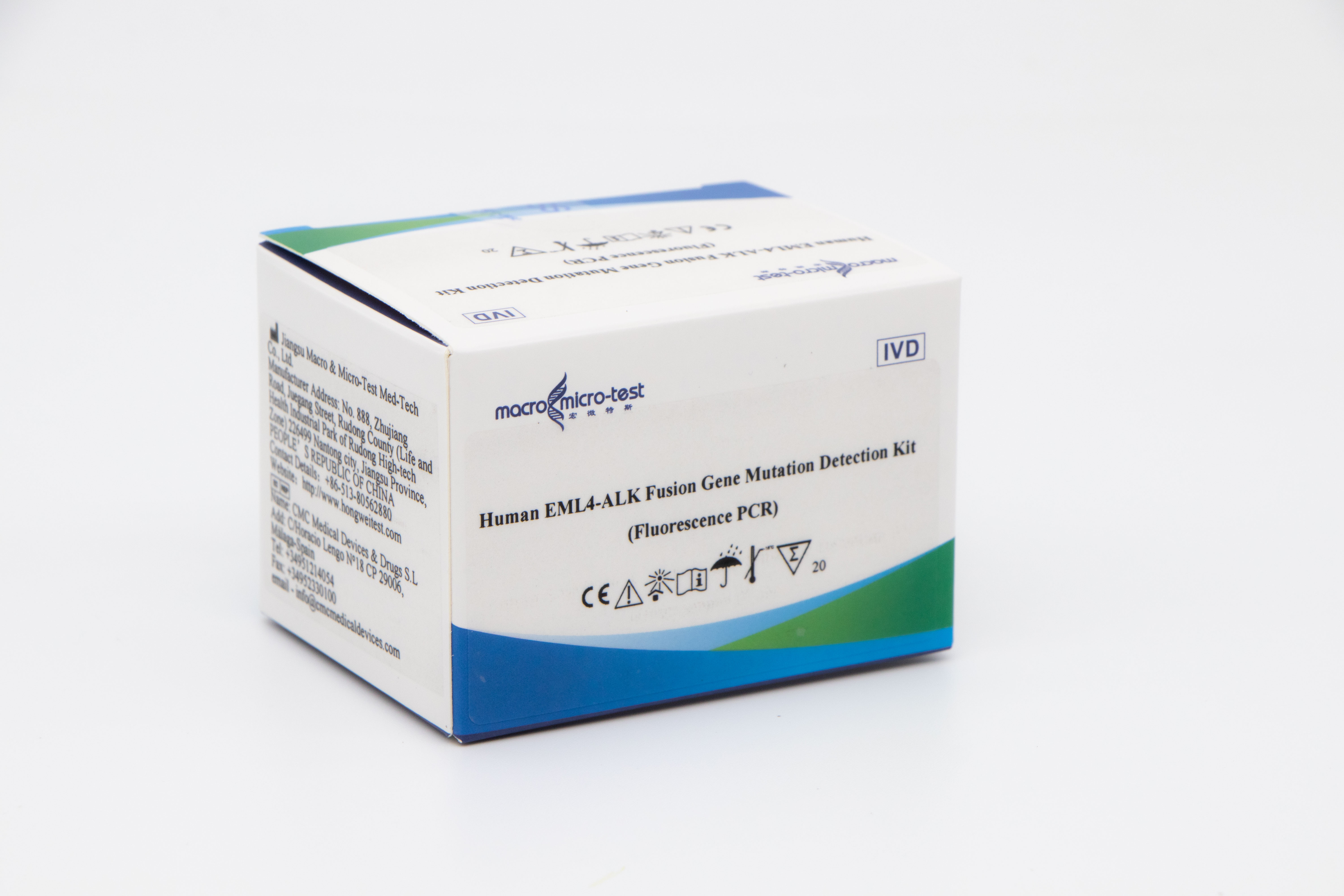
Humán EML4-ALK fúziós génmutáció-kimutatási készlet (fluoreszcencia PCR)
Ez a készlet az EML4-ALK fúziós gén 12 mutációtípusának kvalitatív kimutatására szolgál emberi, nem kissejtes tüdőrákos betegek mintáiban in vitro.
1. A rendszer belső referencia minőségellenőrzést vezet be, amely átfogóan figyelemmel kíséri a kísérleti folyamatot és biztosítja a kísérlet minőségét.
2. Nagy érzékenység: Ez a készlet akár 20 kópia fúziós mutációit is képes kimutatni.
3. Nagy specificitás: Nincs keresztreakció vad típusú humán genomiális DNS-sel és más mutáns típusokkal.
 |  |
Humán ROS1 fúziós génmutáció-kimutatási készlet (fluoreszcencia PCR)
Ez a készlet 14 típusú ROS1 fúziós génmutáció in vitro kvalitatív kimutatására szolgál emberi nem kissejtes tüdőrák mintákban.
1. A rendszer belső referencia minőségellenőrzést vezet be, amely átfogóan figyelemmel kíséri a kísérleti folyamatot és biztosítja a kísérlet minőségét.
2. Nagy érzékenység: Ez a készlet akár 20 kópia fúziós mutációit is képes kimutatni.
3. Nagy specificitás: Nincs keresztreakció vad típusú humán genomiális DNS-sel és más mutáns típusokkal.
 |  |
Humán BRAF gén V600E mutáció detektáló készlet (fluoreszcencia PCR)
Ez a tesztkészlet a BRAF V600E gén mutációjának kvalitatív kimutatására szolgál paraffinba ágyazott emberi melanoma, vastagbélrák, pajzsmirigyrák és tüdőrák szövetmintákban in vitro.
1. A rendszer belső referencia minőségellenőrzést vezet be, amely átfogóan figyelemmel kíséri a kísérleti folyamatot és biztosítja a kísérlet minőségét.
2. Nagy érzékenység: A nukleinsav-reakcióoldat kimutatása stabilan képes kimutatni az 1%-os mutációs arányt 3 ng/μL vad típusú háttér mellett.
3. Nagy specificitás: Nincs keresztreakció vad típusú humán genomiális DNS-sel és más mutáns típusokkal.
 |  |
| Katalógusszám | Termék neve | Specifikáció |
| HWTS-TM012A/B | Humán EGFR gén 29 mutációk detektáló készlet (fluoreszcencia PCR) | 16 teszt/készlet, 32 teszt/készlet |
| HWTS-TM014A/B | KRAS 8 mutáció detektáló készlet (fluoreszcencia PCR) | 24 teszt/készlet, 48 teszt/készlet |
| HWTS-TM006A/B | Humán EML4-ALK fúziós génmutáció-kimutatási készlet (fluoreszcencia PCR) | 20 teszt/készlet, 50 teszt/készlet |
| HWTS-TM009A/B | Humán ROS1 fúziós génmutáció-kimutatási készlet (fluoreszcencia PCR) | 20 teszt/készlet, 50 teszt/készlet |
| HWTS-TM007A/B | Humán BRAF gén V600E mutáció detektáló készlet (fluoreszcencia PCR) | 24 teszt/készlet, 48 teszt/készlet |
| HWTS-GE010A | Humán BCR-ABL fúziós génmutáció-kimutatási készlet (fluoreszcencia PCR) | 24 teszt/készlet |
Közzététel ideje: 2023. április 17.
