2026. március 24-én van a 31. tuberkulózis világnapja. Az Egészségügyi Világszervezet (WHO) az idei globális témát a következőképpen jelölte meg:„Igen! Véget vethetünk a TBC-nek!”, hangsúlyozva, hogy az erős kormányzati vezetés, a tartós politikai elkötelezettség és az összehangolt, több ágazatra kiterjedő fellépés elengedhetetlen a tuberkulózis (TBC) járvány megállításához.

Globális haladás és fennmaradó kihívások
A 2025-ös globális tuberkulózisjelentés szerint a globális tuberkulózis-ellenőrzés jelentős mérföldkövet ért el 2024-ben, mindkettővelaz előfordulási gyakoriság és a halálozási arány csökkenőben vana COVID-19 világjárvány óta először.
Becsült10,7 millió ember2024-ben tuberkulózist diagnosztizáltak náluk, akik közül 54% férfi, 35% nő, 11% pedig gyermek és serdülő volt. Ezen esetek közül körülbelül619 000 (5,8%)HIV-vel is fertőzöttek voltak, és390 000 (3,6%)multirezisztens vagy rifampicin-rezisztens tuberkulózis (MDR/RR-TB) volt.
A tuberkulózis körülbelül1,23 millió haláleset2024-ben továbbra is a vezető fertőző halálok volt világszerte, megelőzve a COVID-19-et. A 2021 és 2023 közötti három évnyi növekedés után a globális tuberkulózis előfordulása közel 2%-kal csökkent 2024-ben, ami a tuberkulózissal kapcsolatos szolgáltatások fokozatos helyreállását tükrözi.[1]
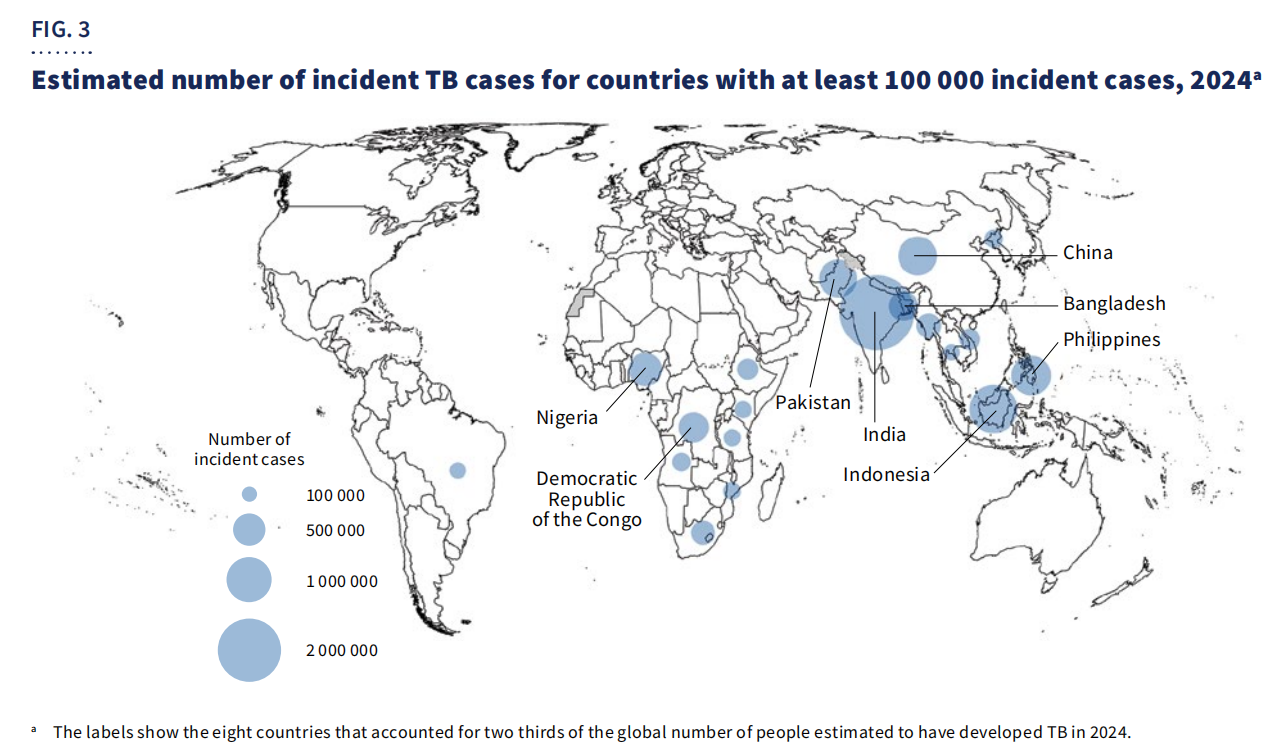
Földrajzilag,Az esetek 67%-ábannyolc országban koncentrálódtak: Indiában, Indonéziában, a Fülöp-szigeteken, Kínában, Pakisztánban, Nigériában, a Kongói Demokratikus Köztársaságban és Bangladesben.
A haladás ellenére a tuberkulózis továbbra is a HIV-vel élők körében a vezető halálokok közé tartozik, és jelentősen hozzájárul az antimikrobiális rezisztenciával összefüggő halálozáshoz. A globális finanszírozás továbbra is hiányos, mindössze5,9 milliárd USD2024-ben elérhető – jóval a vártnál alacsonyabb22 milliárd dolláros éves cél2027-re kitűzve.
Ezek a számok rávilágítanak arra, hogy sürgősen meg kell erősíteni a tuberkulózis-ellenőrzési programokat globálisan, különös tekintettel a diagnosztikához való hozzáférés bővítésére, a kezelési eredmények javítására és a tuberkulózis terjedését befolyásoló társadalmi tényezők kezelésére. A tuberkulózis elleni küzdelem továbbra is erős nemzetközi együttműködést és politikai elkötelezettséget igényel a tuberkulózis elleni stratégia céljainak eléréséhez.
Mycobacterium tuberculosis: Patogenezis és osztályozás
A Mycobacterium tuberculosis (MTB/M. tuberculosis) a tuberkulózisért (TBC) felelős elsődleges és leggyakoribb kórokozó. A légzőrendszeren, az emésztőrendszeren vagy a sérült bőrön és nyálkahártyákon keresztül juthat be az emberi szervezetbe, több szervet is megfertőzve és a TBC különböző formáit okozva. A tüdő-TBC, amely elsősorban cseppfertőzéssel terjed, a TBC-s esetek több mint 80%-át teszi ki. Gyakori tünetek közé tartozik a köhögés, a köpetképződés és a vérköpés. A tüdőben történő fertőzés után a baktérium a véráramon keresztül több rendszerbe is átterjedhet, ami potenciálisan csontrendszeri, húgyúti vagy gyomor-bélrendszeri TBC-hez vezethet.[2]
Az MTB a Mycobacterium nemzetség része, amely magában foglalja:
- Mycobacterium tuberculosis komplex (MTBC): Többek között az M. tuberculosis, M. bovis, M. africanum, M. canettii és M. microti baktériumokat foglalja magában. Míg az M. tuberculosis a TBC elsődleges oka, az M. bovis és az M. africanum is kiválthatja a betegséget.
- Nem tuberkulózisos mikobaktériumok (NTM).
- Mycobacterium leprae, a lepra okozója.
Laboratóriumi diagnosztikai megközelítések
A pontos és időben történő diagnózis elengedhetetlen a hatékony tuberkulózis-ellenőrzéshez. Az Egészségügyi Világszervezet hangsúlyozza, hogyA gyors molekuláris diagnosztikai technológiák alapvetően átalakították a tuberkulózis kimutatását azáltal, hogy lehetővé teszik a kórokozók rendkívül érzékeny és specifikus azonosítását, miközben egyidejűleg kimutatják a gyógyszerrezisztenciát is.[1].
- Mikroszkópia és tenyésztése: A tenyésztés továbbra is az arany standard a TBC diagnózisában, mivel lehetővé teszi az életképes organizmusok végleges azonosítását, és támogatja a gyógyszerérzékenységi vizsgálatot és a genomikai elemzést. A Mycobacterium tuberculosis lassú növekedési üteme miatt azonban az eredmények jellemzően 2-8 hetet igényelnek, ami korlátozza klinikai hasznosságát a sürgős döntéshozatalban.
-Immunológiai vizsgálat: Az immunológiai módszerek, beleértve a tuberkulin bőrtesztet (TST) és az interferon-gamma felszabadulási vizsgálatokat (IGRA), kimutatják a gazdaszervezet immunválaszát a TBC-fertőzésre. Bár hasznosak a látens fertőzés azonosításában, ezek a vizsgálatok nem tudják megbízhatóan megkülönböztetni az aktív és a korábbi fertőzést, ezért korlátozott diagnosztikai specificitásuk van a nagy terhelésű környezetben.
-Molekuláris diagnosztika (NAAT): A DNS-alapú tesztek, mint például a nukleinsav-amplifikáció (NAAT), ajánlottak magas érzékenységük és specificitásuk miatt.
-Célzott következő generációs szekvenálás (tNGS): A célzott szekvenálási technológiák nagy felbontású azonosítást tesznek lehetővé a rezisztenciával összefüggő mutációk esetében. A WHO irányelvei a tNGS-t ajánlják a diagnózis utáni gyógyszerrezisztencia-kimutatás fejlett eszközeként, támogatva a precíziós kezelési stratégiákat [3].
-Metagenomikus következő generációs szekvenálás (mNGS): A metagenomikai szekvenálás lehetővé teszi a kórokozók széles körének elfogulatlan kimutatását előzetes célpontkiválasztás nélkül. Ez a megközelítés különösen értékes összetett vagy nem egyértelmű klinikai esetekben, beleértve a vegyes fertőzéseket és az immunhiányos betegeket, ahol a hagyományos diagnosztika elégtelen lehet.
A WHO továbbá kiemeli, hogy a mikrobiológiai megerősítés elengedhetetlen a megfelelő terápia megkezdéséhez és a betegek kimenetelének javításához, megerősítve a fejlett molekuláris diagnosztika integrálásának fontosságát a tuberkulózis-ellenőrzési programokba [1].
Átfogó molekuláris diagnosztikai megoldások a Macro & Micro-Test-től
1.Multiplex PCR-rel kimutatható a tuberkulózis és a gyógyszerrezisztenciatuberkulózis
| Termékkód | Termék neve | Tanúsítvány |
| HWTS-RT001 | Mycobacterium tuberkulózis DNS-kimutató készlet (fluoreszcencia PCR) | CE |
| HWTS-RT137 | Mycobacterium Tuberculosis Izoniazid Rezisztencia Mutáció Kimutató Készlet (Olvadási Görbe) | CE |
| HWTS-RT074 | Mycobacterium Tuberculosis nukleinsav- és rifampicin-rezisztencia kimutató készlet (olvadási görbe) | CE |
| HWTS-RT102 | Enzimatikus próba izotermikus amplifikációján (EPIA) alapuló nukleinsav-kimutatási készlet Mycobacterium tuberculosis kimutatására | CE |
| HWTS-RT144 | Fagyasztva szárított Mycobacterium Tuberculosis komplex nukleinsav-kimutató készlet (enzimatikus próba izotermikus amplifikációval) | CE |
| HWTS-RT105 | Fagyasztva szárított Mycobacterium Tuberculosis DNS kimutató készlet (fluoreszcens PCR) | CE |
| HWTS-RT147 | Mycobacterium Tuberculosis nukleinsav és rifampicin, izoniazid rezisztencia kimutatására szolgáló készlet (olvadási görbe) | CE |
Amikor erős klinikai gyanú áll fenn a tuberkulózis (TBC) jelenlétére, aHWTS-RT147teszt ajánlott az MTB-fertőzés és a multirezisztens tuberkulózis (MDR-TB) kvalitatív kimutatására. Ez a teszt azonosítja a mutációkat arpoB gén, ami rifampicin (RIF) rezisztenciához és mutációkhoz vezet akatG és InhA gének, amelyek az izoniazid (INH) rezisztenciával hozhatók összefüggésbe. Hatékony, egyszeri tesztet biztosít mind az MTB, mind az MDR-TB kimutatására, belső minőségellenőrzést alkalmazva a téves negatív eredmények minimalizálása érdekében, biztosítva a gyors és pontos eredményeket.
2.PTNseq célzott szekvenálás légúti kórokozók és rezisztencia profilalkotás céljából
| Termékkód | Termék neve | Specifikáció |
| HWKF-TS0001 | PTNseq véráramfertőzés-kórokozó géndúsító készlet | 24 teszt/készlet |
| HWKF-TS0002 | PTNseq központi idegrendszeri fertőzés kórokozó mikroorganizmus géndúsító készlet | 24 teszt/készlet |
| HWKF-TS0003 | PTNseq légúti fertőzés kórokozó géndúsító készlet | 24 teszt/készlet |
| HWKF-AT0003 | PTNseq légúti fertőzést jelző kórokozó mikroorganizmusok automatizált dúsító könyvtárkészítő készlet (ONT) | 24 teszt/készlet |
| HWKF-TS0004 | PTNseq széles spektrumú fertőző kórokozók géndúsító készlet | 24 teszt/készlet |
| HWKF-TS0005 | PTNseq ultraszéles spektrumú fertőző patogén mikroorganizmus géndúsító készlet | 24 teszt/készlet |
| HWKF-TS0151 | Mycobacterium tipizáló és gyógyszerrezisztencia géndúsító készlet (többszörös amplifikációs módszer) | 24 teszt/készlet |
Vegyes légúti fertőzések esetén (beleértve a felső és alsó légúti fertőzéseket, a tuberkulózist és a krónikus légúti betegségeket), vagy ha gyógyszerrezisztencia génanalízisre van szükség (pl. feltételezett gyógyszerrezisztens tuberkulózis esetén), aPTNseq sorozat célzott nagy áteresztőképességű géndetektálásalkalmazható. A fejlett célzott szekvenálási technológiára épülő PTNseq ultra-multiplex PCR-t alkalmaz specifikus célszekvenciák dúsítására, nagy áteresztőképességű szekvenálással és harmadik generációs nanopórus technológiával kombinálva az átfogó kórokozó-azonosítás és a gyógyszerrezisztencia-profilozás érdekében.
A rendszer szabadalmaztatott, nagy specificitású primereket használ a célgének ultra-multiplex amplifikációjához. Saját fejlesztésű adatbázis és intelligens bioinformatikai algoritmusok támogatásával pontos kórokozó-azonosítást, valamint gyógyszerrezisztencia- és virulenciagén-elemzést biztosít. A célzott dúsítás csökkenti a gazda DNS-éből származó interferenciát, javítja az érzékenységet a magas emberi hátterű mintákban, és lehetővé teszi a nehéz célpontok, például aMycobacterium tuberculosis, gombák, intracelluláris baktériumok, RNS-vírusok, valamint rezisztencia- vagy virulenciagének.
A PTNseq eléri a kimutatási határtakár 100 kópia/ml isés borítók175 gyakori légúti kórokozó, köztük 76 baktérium, 73 vírus, 19 gomba, 7 mikoplazma, valamintChlamydia, Rickettsiaés 54 gyógyszerrezisztencia génA testület magában foglalja aMycobacterium tuberculosiskomplex és főbb nem tuberkulózisos mikobaktériumok.
A PTNseq sorozat a nagy érzékenységet a költséghatékonysággal ötvözi, javítja a kórokozók kimutatási arányát és támogatja az egyénre szabott antimikrobiális terápiát, miközben segít mérsékelni az antimikrobiális rezisztenciát. A teljesen automatizált génszekvenálási könyvtár-előkészítő rendszerrel (AIOS) integrálva egyszerűsített, kórházi megoldást kínál, akár 6,5 órás átfutási idővel a mintától az eredményig.

3. Metagenomikai szekvenálás széles spektrumú kórokozók kimutatására
| Termékkód | Termék neve | Specifikáció |
| HWKF-MN0011 | Metagenomikus kórokozó-kimutató készlet (DNS-Illumina) | 24 teszt/készlet |
| HWKF-MN0018 | Metagenomikus kórokozó-kimutató készlet (DNS-MGI) | 24 teszt/készlet |
| HWKF-MN0021 | Metagenomikus kórokozó-kimutató készlet (DNA-ONT) | 24 teszt/készlet |
| HWKF-MN0012 | Metagenomikus kórokozó-kimutató készlet (RNS-Illumina) | 24 teszt/készlet |
| HWKF-MN0019 | Metagenomikus kórokozó-kimutató készlet (RNS-MGI) | 24 teszt/készlet |
| HWKF-MN0022 | Metagenomikus kórokozó-kimutató készlet (RNS-ONT) | 24 teszt/készlet |
| HWKF-MN0013 | Metagenomikus kórokozó-kimutató készlet (DNS+RNS-Illumina) | 24 teszt/készlet |
| HWKF-AYM0013 | Metagenomikus kórokozó-detektáló automatizált könyvtárépítő készlet (DNS+RNS-Illumina) | 24 teszt/készlet |
| HWKF-MN0020 | Metagenomikus kórokozó-kimutató készlet (DNS+RNS-MGI) | 24 teszt/készlet |
| HWKF-MN0023 | Metagenomikus kórokozó-kimutatási készlet (DNS+RNS-ONT) | 24 teszt/készlet |
Amikor a klinikai diagnózis nem egyértelmű,mNGS kórokozó nagy áteresztőképességű gén detektálásaA vizsgálat a betegtől vett különféle mintákon végezhető el, beleértve a bronchoalveoláris lavage folyadékot, a köpetet, a torokváladékot, a vért, a pleurális folyadékgyülem-mintát, a gennyet és a szövetmintákat. Ez a megközelítés metagenomikus szekvenálási technológiát alkalmaz, ahol a különböző minták célzott előkezelésen esnek át, majd üveggyöngyökkel és falbontó enzimekkel nukleinsav-extrakciót végeznek, növelve az extrakció hatékonyságát. A szekvenálás több platformhoz is igazodik, biztosítva a nagy adatmennyiséget a jobb mNGS-érzékenység és összeszerelési integritás érdekében. Az adatokat egy saját fejlesztésű adatbázis és intelligens algoritmusok segítségével elemzik a kimutatás érdekében.több mint 20 000 kórokozó, beleértve a baktériumokat, gombákat, vírusokat és parazitákat, információt nyújtva a feltételezett kórokozó mikroorganizmusokról. Ez a módszer alkalmas nehezen diagnosztizálható, kritikus állapotú vagy legyengült immunrendszerű betegek számára, beleértve a következők azonosítását is:MTBösszetettésNTM, valamint vegyes fertőzések esetén. Jelentősen javítja a kórokozók kimutatási arányát, és segít a célzott klinikai antibiotikum-használat irányításában, lehetővé téve a fertőzés pontos diagnosztizálását.
Következtetés
Bár jelentős előrelépés történt, a tuberkulózis továbbra is jelentős globális egészségügyi kihívás, különösen a gyógyszerrezisztencia, a finanszírozási hiányok és a diagnosztikához való egyenlőtlen hozzáférés összefüggésében.
A WHO hangsúlyozza, hogy a gyors molekuláris diagnosztikához és a fejlett szekvenálási technológiákhoz való hozzáférés bővítése elengedhetetlen a tuberkulózis elleni stratégia céljainak eléréséhez. A folyamatos innovációval, beruházásokkal és globális együttműködéssel a tuberkulózis felszámolása már nem vágyálom, hanem elérhető cél.
Referenciák:
- Egészségügyi Világszervezet. Globális tuberkulózisjelentés 2024/2025: Diagnosztikai tesztelés és kezelés.
- Egészségügyi Világszervezet. WHO kézikönyv a tuberkulózis és a gyógyszerrezisztens tuberkulózis kimutatására szolgáló, WHO által ajánlott molekuláris gyors diagnosztikai tesztek kiválasztásához.
- Egészségügyi Világszervezet. A WHO tuberkulózisra vonatkozó konszolidált irányelvei: 3. modul – Diagnózis (2024. évi frissítés).
Közzététel ideje: 2026. márc. 24.
