I. Áttekintés aESMO2025-ös iránymutatás
2025 augusztusában az ESMO hivatalosan is kiadta a Korai és lokálisan előrehaladott, nem kissejtes tüdőrák: ESMO Klinikai Gyakorlati Útmutató a diagnózishoz, kezeléshez és nyomon követéshez című kiadványt, amely a vezető onkológiai folyóiratban, az Annals of Oncology-ban jelent meg. Ez az első átfogó frissítés a 2017-es verzió óta, és rendkívül hiteles referenciát nyújt az onkológusok számára világszerte.

A tüdőrák incidenciája és halálozási aránya világszerte az összes rosszindulatú daganat közül a legmagasabb. Évente több mint 2,2 millió új esetet és több mint 1,8 millió halálesetet regisztrálnak, így a tüdőrák a rákkal összefüggő halálozások vezető oka mind a férfiak, mind a nők körében. A nem kissejtes tüdőrák (NSCLC) az összes tüdőrákos beteg körülbelül 80-85%-át teszi ki. Ezt a komoly hátteret figyelembe véve a 2025-ös irányelv kiadása új tudományos lendületet ad a klinikai gyakorlatnak, és a biomarker-tesztelési stratégiák frissítése különösen kritikus.
II. A legfontosabb irányelvfrissítések értelmezése
2.1 Biomarker tesztelés: „Opcionális”-tól „Alapvető”-ig
A 2025-ös irányelv mérföldkőnek számító stratégiai kiigazítást hajt végre a biomarker-tesztelés tekintetében. Az irányelv kifejezetten kimondja, hogy a biomarker-tesztelés elengedhetetlen az IB-III. stádiumú NSCLC-ben szenvedő betegek kezelési döntéséhez.
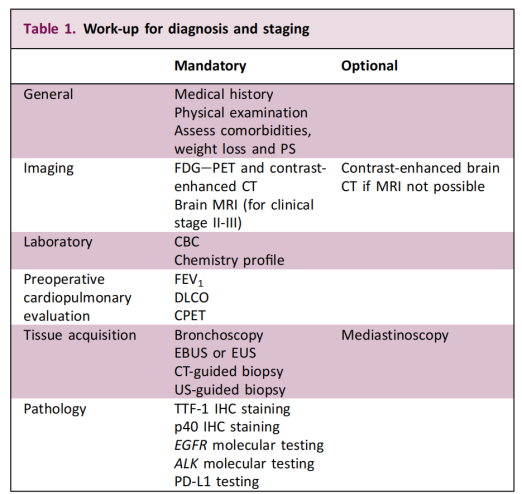
Ez az ajánlás kiterjeszti a molekuláris tesztelést az előrehaladott betegségben szenvedő betegekre való korábbi fókuszról a korai stádiumú, reszekálható esetekre. A fő cél a hajtógénmutációk azonosítása és a személyre szabott precíziós kezelés tudományos alapjainak biztosítása. Az irányelv azt is hangsúlyozza, hogy a biopszia megvalósíthatóságát és a diagnosztikai megközelítést egy multidiszciplináris csapatnak kell meghatároznia a beteg és a daganat jellemzői alapján.
A konkrét vizsgálati stratégiát illetően az irányelv egyértelműen javasolja, hogy a sebészeti döntéshozatal előtt genetikai vizsgálatot végezzenek, és hogy annak legalább az EGFR-re és az ALK-ra kiterjedjen. Ennek az „előzetes vizsgálatnak” a koncepciója mélyreható klinikai jelentőséggel bír a korai stádiumú NSCLC pontos rétegződése és személyre szabott kezelése szempontjából – a vizsgálati eredmények időszerűsége és pontossága közvetlenül meghatározza a későbbi adjuváns terápia megválasztását.
2.2 Terápiás áttörések a vezető onkogén-pozitív korai stádiumú NSCLC kezelésében
A 2025-ös irányelv több jelentős klinikai vizsgálat eredményeit integrálja, hogy egyértelmű precíziós kezelési útvonalat alakítson ki a vezető-onkogén-pozitív, korai stádiumú NSCLC-ben szenvedő betegek számára.
EGFR-mutációt hordozó betegek:A mérföldkőnek számító ADAURA vizsgálat alapján a posztoperatív adjuváns ozimertinib három évig tartó alkalmazása globális standard kezelési móddá vált az EGFR exon 19 deléciókkal vagy exon 21 L858R mutációkkal rendelkező betegeknél. Az ADAURA vizsgálat egy nemzetközi, multicentrikus, randomizált, kontrollált III. fázisú vizsgálat, amely az adjuváns ozimertinib hatékonyságát és biztonságosságát értékeli teljesen reszekált IB-IIIA stádiumú EGFR-mutáns NSCLC betegeknél. A vizsgálat kimutatta, hogy az ozimertinib szignifikánsan javította mind a betegségmentes túlélést, mind a teljes túlélést a placebóhoz képest, ezzel megalapozva az ozimertinib új standard kezelési móddá válását ebben a populációban. Az ADAURA vizsgálat feltáró elemzései azonban azt mutatták, hogy a korai kezelés leállításának körülbelül 36%-át mellékhatások, további 31%-át pedig a beteg döntése okozta. Ez a megállapítás rávilágít a kezelés előtti pontos alapvizsgálatok szükségességére annak biztosítása érdekében, hogy a célzott terápiát olyan betegek kapják, akik tartós előnyökkel járhatnak.
ALK-pozitív betegek:Az ALINA vizsgálat alapján a posztoperatív adjuváns alektinib két évig tartó kezelése ma már a standard kezelés. A III. fázisú, randomizált, nyílt elrendezésű ALINA vizsgálat elsődleges elemzésében az alektinib jelentős betegségmentes túlélési előnyt mutatott a II-IIIA stádiumú populációban, 0,24-es kockázati aránnyal. Az ALINA vizsgálat frissített adatai, amelyeket az ESMO 2025 kongresszuson mutattak be, azt mutatták, hogy ≥3 év követés után az alektinib betegségmentes túlélési előnye „tartós és klinikailag jelentős” maradt, 0,36-os kockázati aránnyal a II-IIIA stádiumú populációban. A legfrissebb jelentett 4 éves teljes túlélési arány elérte a 98,4%-ot, a 4 éves betegségmentes túlélési arány 75,5% volt, és a központi idegrendszeri betegségmentes túlélés is javult, új biztonságossági jelek nélkül. Ezek a robusztus adatok tovább erősítik az adjuváns alektinibet, mint az ALK-pozitív NSCLC reszekciója utáni standard kezelést, és hangsúlyozzák a pontos tesztelés értékét az ilyen betegek azonosításában.
A vizsgálati módszer kiválasztása:A 2025-ös ESMO irányelv kifejezetten felsoroljamultiplex RT-PCR panelvizsgálatokaz RNS-alapú NGS, IHC és FISH mellett az ALK fúzió kimutatásának egyik ajánlott technikai megközelítéseként. Ez azt jelzi, hogy az irányelv alapvető követelménye a klinikai döntések irányítását célzó vizsgálatok elvégzése, nem pedig egy adott vizsgálati platform előírása. Az EGFR és ALK kimutatására összpontosító RT-PCR termékek esetében ez a rugalmas vizsgálati stratégia erős, irányelveken alapuló indoklást nyújt a klinikai gyakorlatban való alkalmazásukra.
III. Precíziós tesztelési műszaki megoldások
A 2025-ös irányelv a tesztelést a műtét előtti döntéshozatali szakaszba helyezi előre, ami magasabbra teszi a lécet a vizsgálat pontossága, érzékenysége és hozzáférhetősége tekintetében. Az alább ismertetett két RT-PCR alapú kimutatási termék technikai szempontból pontosan megfelel az irányelv követelményeinek.
3.1 EGFR mutáció detektáló készlet – Továbbfejlesztett ARMS technológiai platform
Alapvető technológiaA továbbfejlesztett ARMS technológia lehetővé teszi az alacsony gyakoriságú mutáns szekvenciák specifikus amplifikációját magas vad típusú háttérrel szemben.
Három technikai védelmi intézkedés:
-Továbbfejlesztett ARMS → javítja a mutációfelismerést
-Enzimatikus dúsítás → emészti a vad típusú hátteret és feldúsítja a mutáns szekvenciákat
-Hőmérséklet-blokkolás → elnyomja a nem specifikus amplifikációt
TeljesítményÉrzékenység1%-os mutáns allélgyakoriság
Szennyezettség ellenőrzésBeépített belső kontroll + UNG enzim a szennyeződés megelőzésére
Átfutási időZárt csöves működés, kb.120 perc
Minta kompatibilitás:Szövet/folyékony biopsziaminták → megfelel az „előzetes tesztelés” követelményének
Lefedettség:45 mutációaz EGFR 18-21 exonokban, pontosan megegyezve az irányelvekben kiemelt régiókkal (19-es exon deléciók és 21-es exon L858R)
Klinikai alkalmazásKözvetlenül irányítja az EGFR-TKI terápiát
3.2 MMT EML4-ALK fúziós detektáló készlet – RNS-alapú fúziós detektáló megoldás

-Technológiai platformRNS-alapú RT-PCR – a DNS-alapú módszerekkel szembeni előnyöket kínál a fúziók kimutatásában
-RNS-alapú előnyKözvetlenül érzékeli az expresszált fúziós transzkriptumokat, hatékonyan elkerülve a téves negatív eredményeket
-Tanulmányi bizonyítékokAlacsony gyakoriságú ALK fúziók esetén az RT-PCR jelentősen megbízhatóbb, mint a DNS-alapú tesztek.
-ÉrzékenységÉszleli az összeolvadásokat egészen a20 másolat reakciónként
-Változatok lefedettségeBorítók12 gyakori EML4-ALK fúziós variáns(beleértve az 1. variánst ~33%; a 3a/3b variánsokat együtt ~29%)
-Működés és szennyeződés-ellenőrzésZárt kémcső, ~120 perc; beépített folyamatszabályozás + UNG enzim a téves eredmények elkerülése érdekében
-MűszerkompatibilitásKompatibilis a különféle elterjedt valós idejű PCR eszközökkel
-Útmutató igazításaNagymértékben összhangban van az ESMO irányelveivel
IV. A vizsgálatok és az irányelv-ajánlások közötti összhang
A két kimutatási termék nagymértékben összhangban van az ESMO 2025 korai és lokálisan előrehaladott, nem kissejtes tüdőrákra vonatkozó irányelveivel a következő főbb dimenziókban:
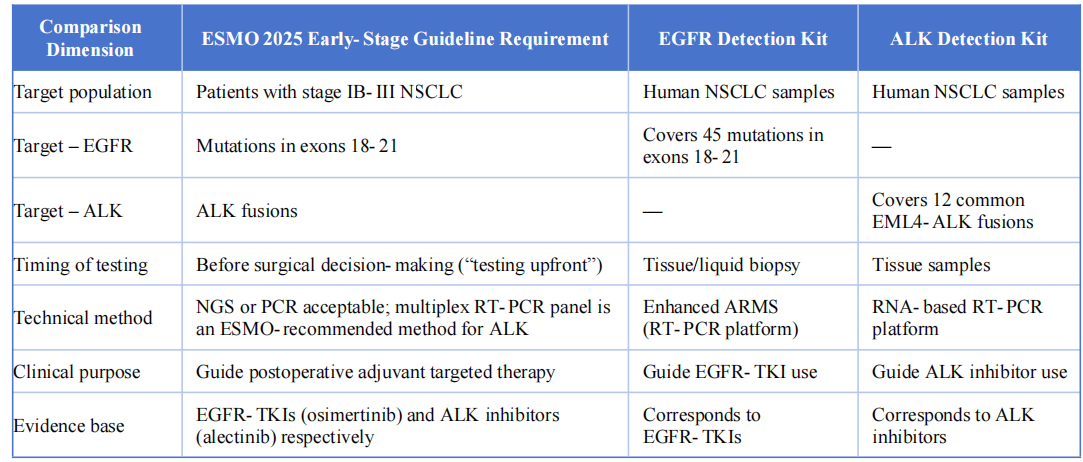
V. Következtetés
Az ESMO 2025 korai stádiumú NSCLC irányelve a precíziós diagnosztika és kezelés új korszakát nyitja meg, amelynek középpontjában a „előzetes tesztelés, pontos célzás és kezelés optimalizálása.„Az EGFR mutáció detektáló készlet és az MMT EML4-ALK fúzió detektáló készlet különböző technikai útvonalakon keresztül felel meg az irányelvek célpontokra, időzítésre és pontosságra vonatkozó követelményeinek.”
Az EGFR készlet továbbfejlesztett ARMS technológiát alkalmaz a célzott mutációk nagy érzékenységű kimutatására korlátozott mintákban, támogatva mind a szöveti, mind a folyékony biopsziát, lehetővé téve az „előzetes tesztelést”.
Az ALK készlet RNS-alapú RT-PCR-en alapul, amely előnyöket kínál a DNS-módszerekkel szemben a fúziók kimutatásában, összhangban az ESMO multiplex RT-PCR panelekre vonatkozó ajánlásával az ALK teszteléshez.
Ez a két termék együttesen egy precíziós vizsgálati megoldást alkot, amely megfelel az ESMO 2025 irányelvnek, és támogatja a személyre szabott adjuváns terápiát a korai stádiumú NSCLC esetén.
Referenciák:
- Zer A, Ahn MJ, Barlesi F és munkatársai. Korai és lokálisan előrehaladott nem kissejtes tüdőrák: ESMO Klinikai Gyakorlati Útmutató a diagnózishoz, kezeléshez és nyomon követéshez. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Közzététel ideje: 2026. május 6.

