A British Journal of Clinical Pharmacology nemrégiben publikálta az Egyesült Királyság Farmakogenomikai Szabályozási Tudományok és Innováció Kiválósági Központja (CERSI PGx) által kidolgozott első klinikai irányelvet, melynek címe: „CYP2C19 genotípus-vizsgálat klopidogrelre: Az Egyesült Királyság farmakogenomikai szabályozási tudományos és innovációs kiválósági központja (CERSI PGx) által kidolgozott irányelv”. Ez a mérföldkőnek számító dokumentum a CYP2C19 genotípus-meghatározás klinikai értékére összpontosít a klopidogrel-terápia irányításában.

A CERSI PGx-ről
A CERSI PGx egyike annak a hét, az Egyesült Királyság kormánya által támogatott szabályozási tudományos és innovációs központnak, amelyek 2025 januárjában indultak. A Liverpooli Egyetem vezeti, és az Innovate UK, az Orvosi Kutatási Tanács (MRC), a Gyógyszer- és Egészségügyi Termékek Szabályozó Ügynöksége (MHRA) és az Élettudományi Hivatal (OLS) közösen finanszírozza. A központ célja, hogy felgyorsítsa a farmakogenomika (PGx) biztonságos és hatékony integrációját a Nemzeti Egészségügyi Szolgálatba (NHS) a főbb megvalósítási akadályok kezelésével. Ez az irányelv a CERSI PGx létrehozása óta kiadott első klinikai útmutató.
Miért fontos a CYP2C19 a klopidogrel esetében?
A CYP2C19 a citokróm P450 enzimcsalád kulcsfontosságú tagja, amely számos gyógyszer metabolikus aktiválásáért vagy inaktiválásáért felelős. A CYP2C19 genetikai polimorfizmusai jelentős egyéni különbségeket okoznak a gyógyszermetabolizmusban, ami befolyásolja a hatékonyságot és a biztonságosságot.
A klopidogrel egy széles körben alkalmazott vérlemezke-gátló szer a trombotikus események megelőzésére koszorúér-betegség, ischaemiás stroke, perifériás artériás betegség és pitvarfibrilláció esetén. Prodrugként a klopidogrel metabolikus aktivációt igényel a CYP2C19 által. Az irányelv a CYP2C19 genotípus alapján ultragyors, gyors, normál, közepes és lassú metabolizálókra osztja az egyéneket. A funkcióvesztéses allélok (pl. CYP2C192 és *3*) hordozói – a közepes és lassú metabolizálók – nem tudják hatékonyan aktiválni a klopidogrelt, ami elégtelen vérlemezke-gátláshoz és a visszatérő trombózis kockázatának növekedéséhez vezet.
A CYP2C192 allél gyakorisága körülbelül 15% az európaiaknál, 30% a dél-ázsiaiaknál, és akár 60% az óceániai őslakos populációknál.
Fő ajánlás: Univerzális CYP2C19 tesztelés klopidogrel esetén
Az irányelv kimondja, hogy az indikációtól függetlenül minden olyan betegnél, akinél a klopidogrel alkalmazását fontolgatják, vizsgálatot kell végezni.CYP2C19genotípus-meghatározás.Az eredmények alapján a vérlemezke-gátló terápiát optimalizálni kell:
-Gyenge metabolizálókkerülniük kell a klopidogrélt, és előnyben kell részesíteniük olyan alternatív gyógyszereket, amelyek nem függnek a CYP2C19 metabolizmusától, például a ticagrelort vagy a prasugrelt.
-Közepes metabolizálókklopidogrel dózisának egyszerű emelése helyett alternatív szereket vagy módosított adagolási rendet is fontolóra kell venni.
Az Egyesült Királyságban a klopidogrel engedélyezett az aterotrombotikus események másodlagos megelőzésére, közepes vagy magas kockázatú átmeneti iszkémiás roham (TIA) vagy enyhe iszkémiás stroke esetén, valamint pitvarfibrilláció esetén az aterotrombotikus és tromboembóliás események megelőzésére.
A klopidogrelen túl: Egyéb gyógyszerek, amelyeknél a CYP2C19 genotípusának meghatározása kritikus fontosságú
A CYP2C19 genotípus-meghatározás értéke messze túlmutat a klopidogrélen. A CYP2C19, mint a gyógyszermetabolizáló fő enzim, kritikus szerepet játszik a vorikonazol, számos antidepresszáns és protonpumpa-gátlók (PPI-k) metabolizmusában is. Számos nemzetközi és nemzeti irányelv javasolja a genotípus-vezérelt individualizálást ezen gyógyszerek esetében.
1. Antidepresszánsok (SSRI-k)
A szelektív szerotonin-visszavétel-gátlók (SSRI-k) – mint például a szertralin, a citalopram és az escitalopram – az első vonalbeli szerek a depresszió kezelésében, és elsősorban a CYP2C19 metabolizálja őket. A CYP2C19 enzim aktivitása közvetlenül meghatározza ezen gyógyszerek plazmakoncentrációját. A lassú metabolizálóknál 30–60%-kal csökken a gyógyszer-clearance, ami hajlamosítja őket olyan mellékhatásokra, mint a QT-intervallum megnyúlása és a szedáció. Az ultragyors metabolizálóknál gyakran szubterápiás plazmakoncentrációk figyelhetők meg, ami késleltetett kezelési válaszhoz és a gyógyszer elhagyásának fokozott kockázatához vezet.
A 2023-as Klinikai Farmakogenetikai Végrehajtási Konzorcium (CPIC) irányelve kimondja, hogy a citalopramot vagy eszcitalopramot szedő lassú metabolizálóknál fokozott a QT-megnyúlás kockázata, és 50%-os dóziscsökkentést javasol. A Holland Farmakogenetikai Munkacsoport (DPWG) 2021-es irányelve azt javasolja, hogy a lassú metabolizálóknak az eszcitalopram maximális adagját 50%-kal csökkentve kell kapniuk, és az ultragyors metabolizálóknak teljesen kerülniük kell az eszcitalopramot. A szertralin esetében a DPWG a lassú metabolizálóknál a napi 75 mg-ot meg nem haladó adagot javasolja.
Fontos kiemelni, hogy a nemrégiben közzétett, a Kínai Pszichiátriai Társaság Precíziós Orvostudományi Együttműködési Csoportja által kidolgozott Kínai Szakértői Konszenzus a Pszichiátriai Farmakogenomikai Vizsgálatokról (2025) kifejezetten tartalmaz ajánlásokat a CYP2C19 genotípus-meghatározására vonatkozóan. A konszenzusos nyilatkozat megjegyzi, hogy a gyógyszermetabolizáló enzimekre (beleértve a CYP2C19-et is) vonatkozó nemzetközi irányelvek, például a CPIC és a DPWG dózismódosítási ajánlásai a kínai populációk esetében hivatkozhatók. Ezért az SSRI-terápia (pl. eszcitalopram) megkezdése előtti CYP2C19 genotípus-meghatározás lehetővé teszi a dózis optimalizálását vagy az alternatív, nem CYP2C19 által metabolizált gyógyszerekre való áttérést, ezáltal precíziós kezelést érve el, javítva a válaszadási arányokat és csökkentve a mellékhatásokat.
2. Protonpumpa-gátlók (PPI-k)
A protonpumpa-gátlókat – beleértve az omeprazolt, a lanszoprazolt és a pantoprazolt – széles körben alkalmazzák savfüggő rendellenességek, például gyomor-nyelőcső reflux betegség és peptikus fekélyek esetén. Anyagcseréjük nagymértékben függ a CYP2C19-től. A különböző CYP2C19 genotípusú betegek jelentős variabilitást mutatnak a protonpumpa-gátlókra adott válaszukban. A funkcióvesztéses allélok (*2, *3) hordozóinál jelentősen megnő a gyógyszerexpozíció, ami fokozhatja a savszuppressziót, de növelheti a mellékhatások kockázatát is. Ezzel szemben a normál metabolizálók plazmakoncentrációja viszonylag alacsonyabb, és gyengébb savszuppressziót tapasztalhatnak, bár az egyéni eltérések továbbra is jelentősek.
A 2020-as CPIC PPI-irányelvek azt tanácsolják, hogy az omeprazolt vagy hasonló gyógyszereket szedő ultragyors metabolizálók túl gyorsan metabolizálják a gyógyszert, ami elégtelen plazmakoncentrációt és gyenge savszuppressziót eredményez. Ezeknél a betegeknél növelni kell az adagot, és monitorozni kell a terápiás választ. A lassú metabolizálóknál a gyógyszerclearance lassú, és a plazmakoncentráció emelkedhet; bár a hatékonyság jobb lehet, a gyógyszertoxicitás lehetősége megnő. A dózis csökkentése és a válasz monitorozása ésszerű megfontolás. Ezért a PPI-terápiát kezdő betegeknél, vagy azoknál, akik gyenge választ vagy mellékhatásokat tapasztalnak, a CYP2C19 genotípus-meghatározás ajánlott az egyénre szabott adagolás irányításához, a hatékonyság optimalizálásához és a mellékhatások minimalizálásához.
3. Vorikonazol
A vorikonazol egy széles spektrumú gombaellenes szer, amelyet súlyos gombás fertőzések, például invazív aszpergillózis kezelésére alkalmaznak. Szűk terápiás ablakkal rendelkezik: a túlzottan magas plazmakoncentráció növeli a májkárosodás és a látászavarok kockázatát, míg az alacsony koncentráció a kezelés sikertelenségét eredményezi. A vorikonazol metabolizmusát elsősorban a CYP2C19 közvetíti, és a genetikai polimorfizmusok jelentős hatással vannak plazmakoncentrációjára.
A CPIC 2016-ban közzétett egy külön irányelvet a CYP2C19-ről és a vorikonazolról. Ez kimondja, hogy az ultragyors metabolizálóknál csökkent a vorikonazol mélyponti koncentrációja, és gyakran nem érik el a célzott terápiás szintet. A lassú metabolizálóknál emelkedett a mélyponti koncentráció, és jelentősen megnő a mellékhatások kockázata. A CPIC irányelv a genotípus alapján specifikus adagolási ajánlásokat tartalmaz. Például a felnőtt ultragyors metabolizálóknak alternatív, első vonalbeli szereket kell kapniuk, amelyek nem függenek a CYP2C19 metabolizmusától, például izavukonazolt, liposzomális amfotericin B-t vagy pozakonazolt. Ezért a vorikonazol-terápia előtti CYP2C19 genotípus-meghatározás lehetővé teszi az egyénre szabott adagolást, és csökkenti a gyógyszerrel összefüggő mellékhatások előfordulását.
Klinikai jelentőség: A gyógyszerek megbízhatóbbá tétele
Az újonnan kiadott irányelv ismét a precíziós orvoslás élvonalába helyezi a CYP2C19 genotípus-meghatározást. Fontos azonban felismerni, hogy a CYP2C19 genotípus-meghatározás klinikai alkalmazásai messze túlmutatnak a klopidogrelen – a vorikonazoltól (gombaellenes szer) és az SSRI-ktől (antidepresszánsok) a savcsökkentő protonpumpa-gátlókig. A CYP2C19 genotípus „iránytűként” szolgál a gyógyszeres terápia számára.
Ahogy a precíziós orvoslás egyre szélesebb körben elfogadottá válik, egyre több mérvadó irányelv építi be a CYP2C19 genotípus-meghatározást a rutin gyógyszeres munkafolyamatokba. A betegek számára a saját CYP2C19 genotípusuk ismerete segít megérteni az egyéni gyógyszerválasz profiljukat, és lehetővé teszi a közös döntéshozatalt orvosukkal a megfelelőbb kezelési terv kidolgozása érdekében. A klinikusok számára az objektív genetikai teszteredmények integrálása a felírási döntésekbe hatékony eszköz a kezelés minőségének javítására és a betegbiztonság garantálására.
Makro- és mikroteszt'sCYP2C19 genotípus-meghatározási oldat
A Macro & Micro Test egy CYP2C19 genotípus-meghatározó készletet kínál, amely egy továbbfejlesztett amplifikációs refrakter mutációs rendszeren (ARMS) alapul, Taqman próbákkal kombinálva, a következő tulajdonságokkal:
-Átfogó allél lefedettség– észleliCYP2C192, *3 és *17hiányzó kulcsfontosságú változatok nélkül.
-Szigorú minőségellenőrzés– negatív/pozitív kontrollokat, belső kontrollt és UDG enzimet tartalmaz a négyszintű minőségellenőrzéshez a pontos eredmények biztosítása érdekében.
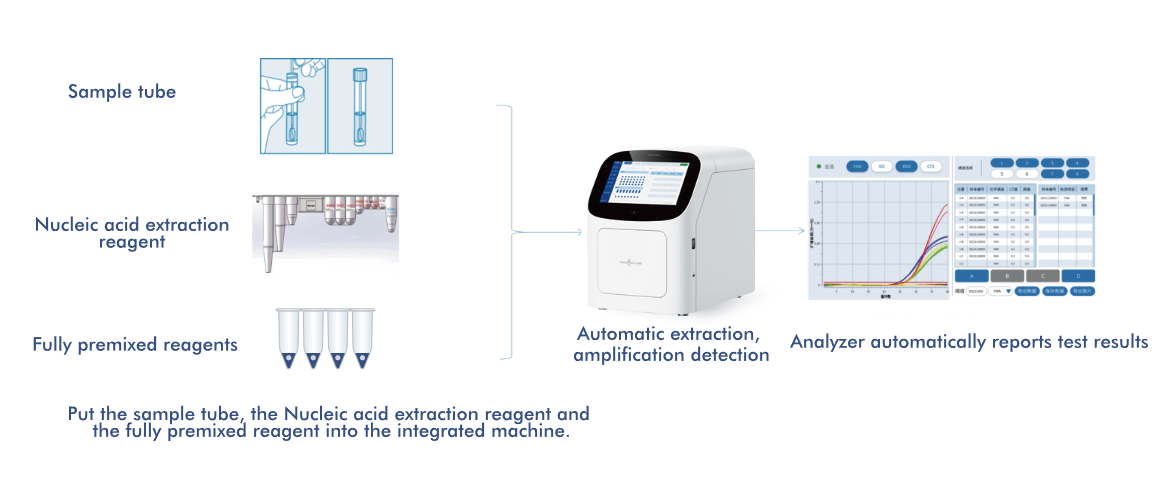
-Automatizált extrakció– kompatibilis a Macro & Micro-Test teljesen automatizált nukleinsav-kivonójával, javítva a munkafolyamatok hatékonyságát.
-Széleskörű kompatibilitás– működik a piacon kapható legelterjedtebb valós idejű PCR eszközökkel, beleértve az ABI 7500 Hongshi SLAN 96P-t is.
-Automatizált eredményértelmezés– dedikált elemzőszoftver (ABI 7500, SLAN 96P stb. készülékeken) lehetővé teszi az eredmények automatikus értelmezését, növelve a hatékonyságot.
-POCT-ready automatizálás– A HWTS AIO800 teljesen automatizált nukleinsav-amplifikációs analizátor lehetővé teszi a „minta be, eredmény ki” működést.
A farmakogenomika folyamatos fejlődésével a CYP2C19 genotípus-meghatározás várhatóan egyre több beteg számára lesz előnyös, a precíziós orvoslást a koncepciótól a rutin klinikai gyakorlattá emelve. Az újonnan közzétett CERSI PGx irányelv megerősíti a CYP2C19 tesztelés kritikus szerepét nemcsak a klopidogrel, hanem a gyógyszerek egyre bővülő listájának, köztük az antidepresszánsok, a protonpumpa-gátlók és a vorikonazol esetében is. A genotípus-vezérelt gyógyszerrendelés széles körű elterjedésének elősegítése érdekében elengedhetetlenek a megbízható és felhasználóbarát tesztelési megoldások. A Macro & Micro-Test farmakogenomikai tesztelési portfóliója, amely átfogó alléllefedettséget, robusztus minőségellenőrzést és automatizálásra kész platformokat tartalmaz, célja, hogy támogassa az egészségügyi szolgáltatókat a precíziós orvoslás bevezetésében és végső soron a betegek egészségének védelmében.
Kapcsolódó termékek:
Referenciák:
1. Lima JJ, Thomas CD, Barbarino J és munkatársai. Klinikai Farmakogenetikai Végrehajtási Konzorcium (CPIC) irányelve a CYP2C19 és a protonpumpa-gátlók adagolásához. Clin Pharmacol Ther. 2020. doi:10.1002/cpt.20151.
2. Lee CR, Luzum JA, Sangkuhl K és munkatársai. Klinikai Farmakogenetikai Végrehajtási Konzorcium Irányelve a CYP2C19 genotípus és a klopidogrel terápia tekintetében: 2022-es frissítés. Clin Pharmacol Ther. 2022. doi:10.1002/cpt.25261.
3. Nemzeti Egészségügyi és Gondozási Kiválósági Intézet (NICE). CYP2C19 genotípus-tesztelés a klopidogrel ischaemiás stroke vagy átmeneti ischaemiás roham utáni alkalmazásának iránymutatására. Diagnosztikai útmutató DG59. Megjelent: 2024. július 31.
4. A Kínai Pszichiátriai Társaság Precíziós Orvostudományi Kutatási Együttműködési Csoportja. Szakértői konszenzus a pszichiátriai farmakogenomikai vizsgálatokról (2025) [Zhonghua Jing Shen Ke Za Zhi].Kínai Pszichiátriai Folyóirat. 2025;58(6):434-445. doi:10.3760/cma.j.cn11366120240611-00181
5. Dello Russo C, Frater I, Kuruvilla R és munkatársai. CYP2C19 genotípusvizsgálat klopidogrelre: Az Egyesült Királyság farmakogenomikai szabályozási tudományok és innováció kiválósági központja (CERSI-PGx) által kidolgozott irányelv. Br J Clin Pharmacol. 2025. DOI: 10.1093/bjcp/…
6. Moriyama B, Owusu Obeng A, Barbarino J és munkatársai. Klinikai Farmakogenetikai Végrehajtási Konzorcium (CPIC) irányelvei a CYP2C19 és a vorikonazol terápiához. Clin Pharmacol Ther. 2017;102(1):45-51. doi:10.1002/cpt.595.
7. Bousman CA, Stevenson JM, Ramsey LB és munkatársai. Klinikai Farmakogenetikai Végrehajtási Konzorcium (CPIC) irányelve a CYP2D6, CYP2C19, CYP2B6, SLC6A4 és HTR2A genotípusokra és a szerotonin-visszavétel-gátló antidepresszánsokra vonatkozóan. Clin Pharmacol Ther. 2023;114(1):51-68. doi:10.1002/cpt.2903.
8. Brouwer JMJL, Nijenhuis M, Soree B és munkatársai. A Holland Farmakogenetikai Munkacsoport (DPWG) irányelvei a CYP2C19 és CYP2D6, valamint az SSRI-k közötti gén-gyógyszer kölcsönhatásról. Eur J Hum Genet. 2021. doi:10.1038/s41431-021-00894-2.
Közzététel ideje: 2026. április 22.