1. A méhnyakrák globális terhe és a szűrés kihívásai
A méhnyakrák továbbra is jelentős globális közegészségügyi kihívás, annak ellenére, hogy hatékony szűréssel és korai beavatkozással nagyrészt megelőzhető. Az Egészségügyi Világszervezet (WHO) szerint 2022-ben világszerte becslések szerint 662 000 új eset és 349 000 haláleset történt, amivel a negyedik leggyakoribb rákbetegség és a negyedik vezető halálok a nők körében a rákkal összefüggő halálozásban. A betegségteher aránytalanul koncentrálódik az alacsony és közepes jövedelmű országokban (LMIC), ahol az előfordulási és halálozási arányok jelentősen magasabbak, mint a magas jövedelmű országokban. Ezek elsősorban a magas színvonalú szűrőprogramok, valamint a rákmegelőző elváltozások hatékony felismerésének és kezelésének hiányából fakadnak, amit súlyosbítanak a következők:
-Hiányzó vagy gyenge szűrőinfrastruktúra:Hozzáférhető, minőségbiztosított szűrőszolgáltatások hiánya.
-Erőforrás-korlátok:Korlátozott laboratóriumi infrastruktúra, hűtőlánc-logisztika és megbízható áramellátás.
-Munkaerőhiány:Képzett laboratóriumi és klinikai személyzet hiánya.
-Késések és az utánkövetés elmaradása:A mintavétel és az eredmények elérhetősége között eltelt idő eltelik, ami késedelmekhez vezethet a klinikai ellátásban, vagy a betegek követési idő csökkenéséhez vezethet[1].
2. A méhnyakrák etiológiája és molekuláris alapjai
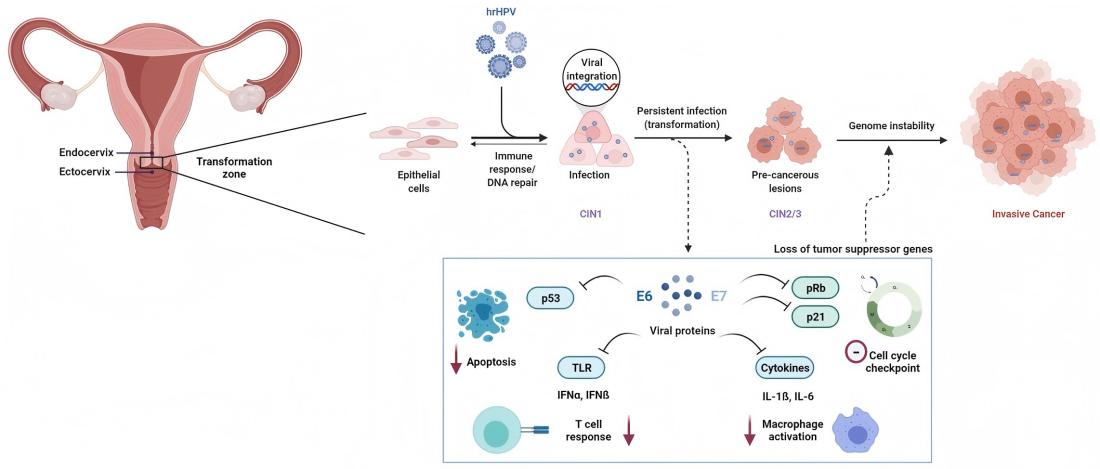
A méhnyakrák kialakulásának egyik szükséges oka a magas kockázatú humán papillomavírus (HR-HPV) tartós fertőzése. A több mint 200 azonosított HPV-genotípus közül legalább 12 típust a Nemzetközi Rákkutató Ügynökség (IARC) rákkeltőnek (1. csoport) minősített.
Molekuláris szinten a HPV által közvetített karcinogenezist elsősorban az E6 és E7 vírusonkoproteinek vezérlik. Az E6 elősegíti a p53 tumorszupresszor fehérje lebontását, míg az E7 funkcionálisan inaktiválja a retinoblasztóma fehérjét (Rb), ami a sejtciklus szabályozási zavarához és rosszindulatú transzformációhoz vezet.
3. WHO által ajánlott szűrési stratégiák
Az Egészségügyi Világszervezet a HPV nukleinsav-tesztet (NAT) ajánlja a méhnyakrák megelőzésének elsődleges szűrőmódszereként.
Általános lakosság:HPV DNS vagy mRNS alapú NAT-ok
HIV-vel élő nők:HPV DNS-alapú NAT-ok
Szűrési intervallumok:
30–65 éves nők: 5–10 évente
HIV-vel élő nők: 3-5 évente
A citológiai alapú módszerekkel összehasonlítva a HPV-tesztelés kimutatjanagyobb érzékenységés biztosítjakiváló negatív prediktív érték, lehetővé téve a hosszabb és költséghatékonyabb szűrési intervallumokat.
4. WHO céltermékprofil HPV szűrővizsgálatokhoz
A WHO kidolgozott egyCéltermékprofil (TPP)decentralizált és erőforrás-korlátozott környezetben történő használatra szánt HPV szűrővizsgálatokhoz.[1]
Főbb jellemzők a következők:
-Kompatibilitás az önállóan gyűjtött mintákkal
-Több magas kockázatú HPV genotípus (≥12 típus) kimutatása
-Nem laboratóriumi képzésben részesült személyzet általi kezelés
- Az eredmények egyetlen klinikai konzultáción belül elérhetők
Ezek a kritériumok támogatják az ellátás helyszínén történő tesztelést és a „szűrés és kezelés” stratégiákat.
5. Teljesen automatizált, magas kockázatú HPV-észlelő platform
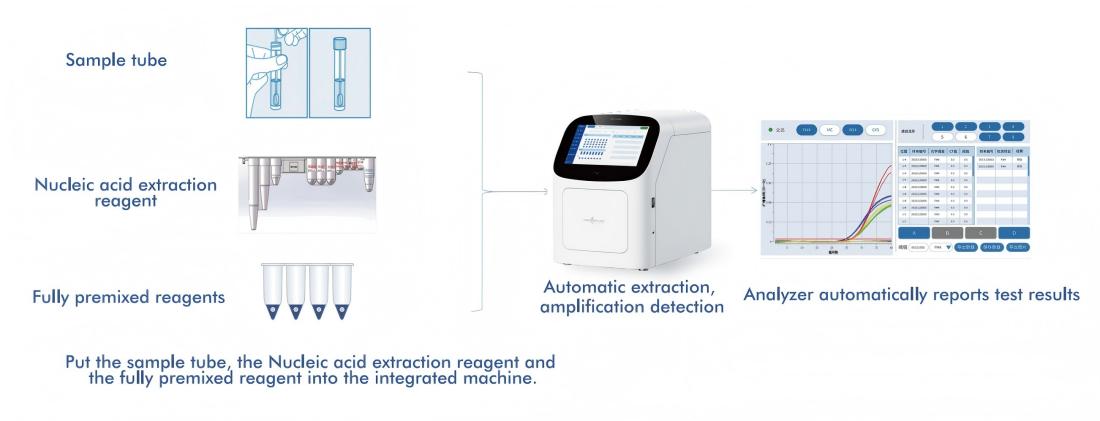
A Macro & Micro-Test AIO800 rendszere biztosítja a következőket:egy teljesen automatizált mintától a válaszig terjedő munkafolyamata nukleinsav-kivonás, -amplifikáció és -kimutatás integrálása a WHO által ajánlott szűrési stratégiákkal összhangban.
5.1 Automatizált mintavételtől a válaszadásig tartó munkafolyamat
A platform egyetlen, zárt rendszerbe integrálja a nukleinsav-kivonást, -amplifikációt és -detektálást, minimális kezelői beavatkozást igényelve. Ez a kialakítás:
-Csökkenti a speciális laboratóriumi személyzettől való függőséget
-Minimalizálja a folyamat változékonyságát és a szennyeződés kockázatát
-Lehetővé teszi a telepítést decentralizált egészségügyi intézményekben
Ugyanakkor az átviteli kapacitása támogatja a központosított laboratóriumokban való alkalmazást, megkönnyítve a nagyszabású szűrőprogramokat.
5.2 Széleskörű genotípus-meghatározási lefedettség
A rendszer 14 magas kockázatú HPV-típust észlel, beleértve az IARC által besorolt mind a 12 rákkeltő típust (HPV16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 és 59), valamint a HPV66-ot és HPV68-at.
Fontos, hogy biztosítjatípusspecifikus genotípus-meghatározáseredményeket, lehetővé téve a kockázatbecslést és a pontosabb klinikai ellátást.
5.3 Analitikai érzékenység és klinikai következmények
A 300 kópia/ml kimutatási határértékkel a rendszer képes azonosítani az alacsony szintű HPV-fertőzést, amely hozzájárul a következőkhöz:
- Klinikailag releváns fertőzések korábbi felismerése
-Javított negatív prediktív érték
-Támogatás a meghosszabbított szűrési intervallumokhoz
5.4 Önmintavételezés támogatása
A platform mindkettővel kompatibilisnyaki tamponminták és önként gyűjtött vizeletmintáka WHO ajánlásaival való összhang megteremtése a szűrővizsgálatok igénybevételét akadályozó főbb akadályok kezelése érdekében, beleértve:
-Korlátozott hozzáférés az egészségügyi intézményekhez
-Szociokulturális korlátok
-A páciens kellemetlensége a klinikus által végzett mintavétellel kapcsolatban
Kimutatták, hogy az önmintavétel növeli a szűrőprogramokban való részvételt, különösen az alulszolgáltatott populációk körében.
5.5 Liofilizált reagens technológia szobahőmérsékleten történő tároláshoz
Az erőforrás-korlátozott környezetben való alkalmazhatóság további javítása érdekében a rendszer magában foglalja a következőket:liofilizált (fagyasztva szárított) reagensekkörnyezeti hőmérsékleten stabilak, számos működési előnnyel járva:
-Hűtőlánc-függetlenség: Nincs szükség hűtött szállításra és tárolásra
-Fokozott stabilitás: Megőrzi a reagensek integritását változó környezeti feltételek mellett is
-Egyszerűsített logisztika: Csökkenti az infrastrukturális követelményeket és az üzemeltetési költségeket
- Fokozott hozzáférhetőség: Megkönnyíti a telepítést távoli vagy alulszolgáltatott régiókban
6. Következtetés
A citológiai alapú szűrésről a HPV-alapú molekuláris tesztelésre való áttérés paradigmaváltást jelent a méhnyakrák megelőzésében. Azzal, hogy a betegség kiváltó okát, és nem a morfológiai változásokat célozza meg, a HPV-tesztelés lehetővé teszikorábbi és érzékenyebb észlelésa veszélyeztetett egyének közül.
Továbbá a teljesen automatizált molekuláris diagnosztikai platformok gyakorlati megközelítést kínálnak a szűrések lebonyolításában meglévő akadályok leküzdésére. Azáltal, hogymagas analitikai teljesítmény egyszerű működtetéssel és az önmintavétel támogatásával,Az AIO800 programban megvan a lehetőség a szűrés lefedettségének bővítésére, a korai felismerés javítására és a méhnyakrák globális terhének csökkentésére.
Referenciák:
1. Egészségügyi Világszervezet. Célzott termékprofilok humán papillomavírus szűrőtesztekhez a méhnyakrák-megelőző állapotok és a méhnyakrák kimutatására. Genf: WHO; 2024.
Közzététel ideje: 2026. márc. 28.