Humán EGFR gén 29 mutációk
Termék neve
HWTS-TM0012A-Humán EGFR gén 29 mutáció detektáló készlet (fluoreszcencia PCR)
Járványtan
A tüdőrák világszerte a rákos halálesetek vezető okává vált, komolyan veszélyeztetve az emberi egészséget. A nem kissejtes tüdőrák a tüdőrákos betegek körülbelül 80%-át teszi ki. Az EGFR jelenleg a legfontosabb molekuláris célpont a nem kissejtes tüdőrák kezelésében. Az EGFR foszforilációja elősegítheti a tumorsejtek növekedését, differenciálódását, invázióját, áttétképződését, antiapoptózisát és elősegítheti a tumor angiogenezist. Az EGFR tirozin-kináz inhibitorok (TKI) blokkolhatják az EGFR jelátviteli útvonalat az EGFR autofoszforilációjának gátlásával, ezáltal gátolják a tumorsejtek proliferációját és differenciálódását, elősegítik a tumorsejtek apoptózisát, csökkentik a tumor angiogenezist stb., így célzott terápiát érhetnek el. Számos tanulmány kimutatta, hogy az EGFR-TKI terápiás hatékonysága szorosan összefügg az EGFR génmutáció állapotával, és specifikusan gátolhatja az EGFR génmutációval rendelkező tumorsejtek növekedését. Az EGFR gén a 7-es kromoszóma rövid karján (7p12) található, teljes hossza 200 kb, és 28 exonból áll. A mutált régió főként a 18-21. exonokban található, a 746-753. kodonok deléciós mutációja a 19-es exonon körülbelül 45%-ot, az L858R mutáció pedig a 21-es exonon körülbelül 40-45%-ot tesz ki. Az NCCN nem kissejtes tüdőrák diagnosztizálására és kezelésére vonatkozó irányelvei egyértelműen kimondják, hogy az EGFR génmutáció-vizsgálat szükséges az EGFR-TKI beadása előtt. Ez a tesztkészlet az epidermális növekedési faktor receptor tirozin-kináz inhibitor (EGFR-TKI) gyógyszerek beadásának útmutatójaként szolgál, és alapul szolgál a személyre szabott orvosláshoz nem kissejtes tüdőrákban szenvedő betegek számára. Ez a készlet kizárólag az EGFR gén gyakori mutációinak kimutatására szolgál nem kissejtes tüdőrákban szenvedő betegeknél. A teszteredmények csak klinikai referenciaként szolgálnak, és nem használhatók fel a betegek egyénre szabott kezelésének kizárólagos alapjául. A klinikusoknak figyelembe kell venniük a beteg állapotát, a gyógyszeres javallatokat és a kezelést. A reakció és egyéb laboratóriumi vizsgálati mutatók, valamint egyéb tényezők a teszteredmények átfogó megítéléséhez használatosak.
Csatorna
| Családi létszám | IC reakciópuffer, L858R reakciópuffer, 19del reakciópuffer, T790M reakciópuffer, G719X reakciópuffer, 3Ins20 reakciópuffer, L861Q reakciópuffer, S768I reakciópuffer |
Műszaki paraméterek
| Tárolás | Folyékony: ≤-18 ℃ sötétben; Liofilizált: ≤30 ℃ sötétben |
| Felhasználhatósági idő | Folyékony: 9 hónap; Liofilizált: 12 hónap |
| Mintatípus | friss daganatszövet, fagyasztott patológiai metszet, paraffinba ágyazott patológiai szövet vagy metszet, plazma vagy szérum |
| CV | <5,0% |
| LoD (mérési határérték) | 3 ng/μL vad típusú háttérben nukleinsav-reakcióoldat-detektálás, stabilan kimutatható 1%-os mutációs arány |
| Specifikusság | Nincs keresztreaktivitás a vad típusú humán genomiális DNS-sel és más mutáns típusokkal |
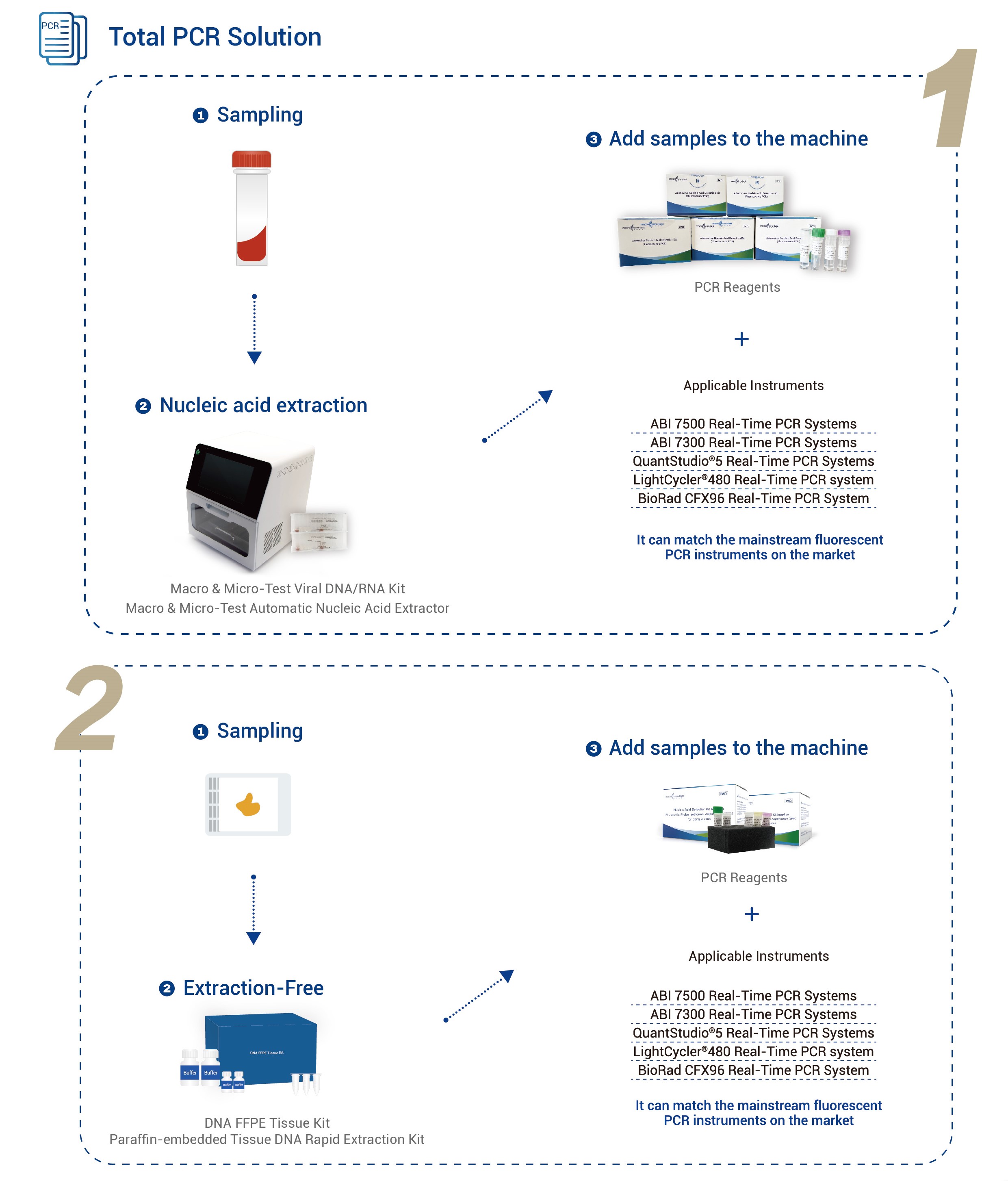
| Alkalmazható eszközök | Applied Biosystems 7500 valós idejű PCR rendszerekApplied Biosystems 7300 valós idejű PCR rendszerek QuantStudio® 5 valós idejű PCR rendszerek LightCycler® 480 valós idejű PCR rendszer BioRad CFX96 valós idejű PCR rendszer |